메뉴
KR | KRW
KR | KRW
Sorry, we couldn't find anything on our website containing your search term.
세균 배양 정량화 방법 - CFU와 OD부터 계수 챔버까지
실험실 아카데미
- 미생물학
- 생명공학
- 바이오프로세싱
- 보건 및 의료
- 제약
- 분자생물학
- 식음료
- Cell Culture
- 효율성
- 미생물 배양
- Cell Culture 소모품
- 바이오 프로세스
- 논문
소개
대부분의 표준 실험 절차와 분석법에서는 연구자의 정확한 세균 세포 계수나 세균 세포 밀도 측정이 먼저 선행되어야 하는 경우가 많습니다. 세포 계수는 세포 성장 추적, 형질전환 및 선택 저항성 평가, 후속 연구를 위한 세포 접종 그리고 세포 기반 분석을 위한 준비 과정에서 매우 중요합니다. 특히 이후에 수행되는 정량적 측정의 신뢰성을 확보하기 위해서는 세균 세포 계수가 정확하고 일관되게 이루어져야 합니다.
이 글에서는 세균 세포를 수동으로 계수하는 각 방법을 개략적으로 살펴보고 각각의 장점과 한계를 알아봅니다. 단백질 발현을 위한 회분식 배양 수행, 형질전환 실험 준비 또는 다양한 자극에 대한 세포의 정량적 반응 측정 모두 이러한 세포 계수법 중 적어도 한 가지는 반드시 필요한 경우가 많습니다. 이 글을 읽고 나면 자신의 연구에 가장 적합한 방법이 무엇인지 찾을 수 있을 것입니다.
대부분의 표준 실험 절차와 분석법에서는 연구자의 정확한 세균 세포 계수나 세균 세포 밀도 측정이 먼저 선행되어야 하는 경우가 많습니다. 세포 계수는 세포 성장 추적, 형질전환 및 선택 저항성 평가, 후속 연구를 위한 세포 접종 그리고 세포 기반 분석을 위한 준비 과정에서 매우 중요합니다. 특히 이후에 수행되는 정량적 측정의 신뢰성을 확보하기 위해서는 세균 세포 계수가 정확하고 일관되게 이루어져야 합니다.
이 글에서는 세균 세포를 수동으로 계수하는 각 방법을 개략적으로 살펴보고 각각의 장점과 한계를 알아봅니다. 단백질 발현을 위한 회분식 배양 수행, 형질전환 실험 준비 또는 다양한 자극에 대한 세포의 정량적 반응 측정 모두 이러한 세포 계수법 중 적어도 한 가지는 반드시 필요한 경우가 많습니다. 이 글을 읽고 나면 자신의 연구에 가장 적합한 방법이 무엇인지 찾을 수 있을 것입니다.
자세히 보기
집락 형성 단위(CFU)
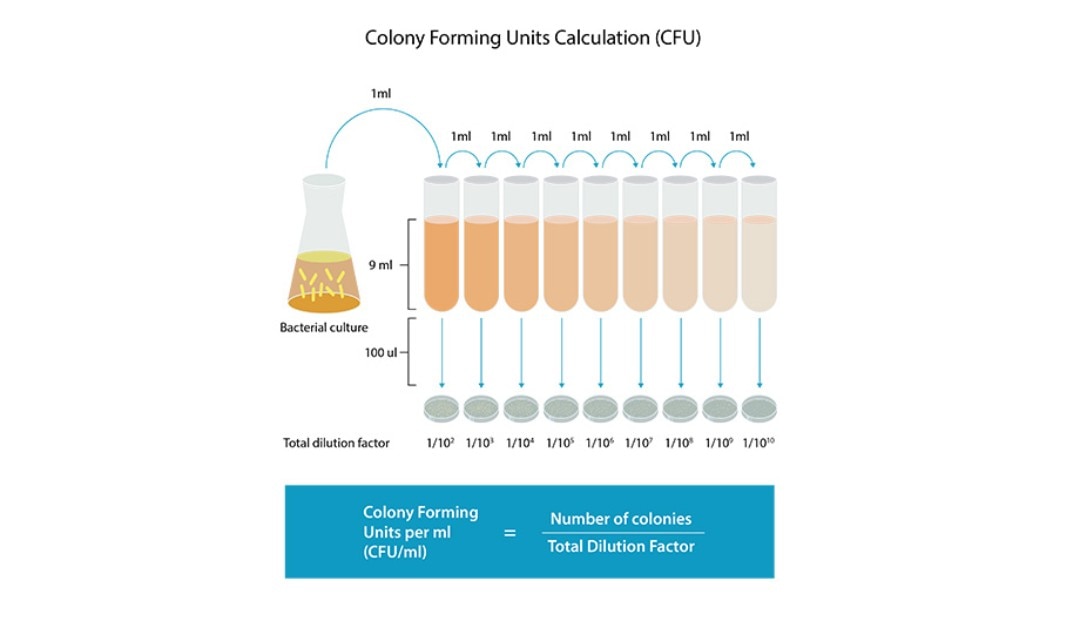
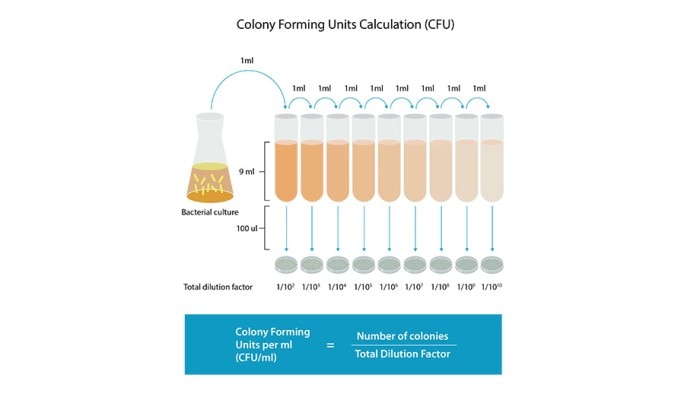
CFU는 배지 위에서 성장할 수 있는 모든 미생물의 개별 집락 수를 의미하며, 생존 가능한 세균 세포를 직접적으로 측정하는 지표입니다. CFU의 표준 측정 단위는 배양액 1 mL당 존재하는 배양 가능 미생물 수(CFU / mL)이며, 그림 1에서처럼 연속 희석법과 도말 배양법을 통해 측정합니다.
CFU는 배지 위에서 성장할 수 있는 모든 미생물의 개별 집락 수를 의미하며, 생존 가능한 세균 세포를 직접적으로 측정하는 지표입니다. CFU의 표준 측정 단위는 배양액 1 mL당 존재하는 배양 가능 미생물 수(CFU / mL)이며, 그림 1에서처럼 연속 희석법과 도말 배양법을 통해 측정합니다.
자세히 보기
일반적인 방법:
예를 들어, 희석 배수 1:100인 배지에서 150개의 집락을 계수했고, 해당 배지에 100 µL를 도말한 경우 다음과 같이 계산합니다.
총 DF = 0.1 mL x 1/100 (또는 0.01) = 0.001
총 CFU = 150 / 0.001 = 150,000 CFU / mL
장점: 전문 장비가 필요 없는 간단한 방법입니다.
단점: 집락 형성에시간이 걸리기 때문에 매우 느립니다.
- 회분식 배양액을 1:10 비율의 연속 희석으로 희석합니다. 이전 희석액 1 mL를 멸균 증류수 9 mL가 들어 있는 다음 튜브로 옮깁니다.
- 적절한 성장 배지가 포함된 한천 배지 위에 100 µL를 피펫팅한 다음, 셀 스프레더를 사용해 고르게 도말합니다.
- 배지에 희석 배수(DF)를 표시하고 하룻밤 동안(또는 필요한 만큼) 배양합니다. (DF = 총 희석 부피/시료 부피)
- 집락 수가 적절한 배지를 선택합니다(집락 수 30~300개 사이).
- 이제 세포 계수를 수행합니다! 각 배지에서 관찰되는 집락 수를 셉니다.
- 각 배지의 CFU를 구한 다음, 다음 계산을 수행합니다.
예를 들어, 희석 배수 1:100인 배지에서 150개의 집락을 계수했고, 해당 배지에 100 µL를 도말한 경우 다음과 같이 계산합니다.
총 DF = 0.1 mL x 1/100 (또는 0.01) = 0.001
총 CFU = 150 / 0.001 = 150,000 CFU / mL
장점: 전문 장비가 필요 없는 간단한 방법입니다.
단점: 집락 형성에시간이 걸리기 때문에 매우 느립니다.
자세히 보기
광학 밀도(OD) 측정
광학 밀도는 분광광도계를 사용해 측정하며, 배양액 내 세포 수를 빠르게 추정할 수 있습니다. 이 기법은 미생물 성장 측정을 추정하는 데 널리 사용되며, 발효 과정 동안 세포 성장을 모니터링하는 데 유용한 방법입니다. 세포 성장은 선형적이지 않고 세포의 상태와 환경을 반영하는 여러 성장 단계가 있습니다. 회분식 배양 동안 일반적인 세포 성장 곡선은 네 가지 뚜렷한 성장 단계를 보여줍니다.
광학 밀도는 분광광도계를 사용해 측정하며, 배양액 내 세포 수를 빠르게 추정할 수 있습니다. 이 기법은 미생물 성장 측정을 추정하는 데 널리 사용되며, 발효 과정 동안 세포 성장을 모니터링하는 데 유용한 방법입니다. 세포 성장은 선형적이지 않고 세포의 상태와 환경을 반영하는 여러 성장 단계가 있습니다. 회분식 배양 동안 일반적인 세포 성장 곡선은 네 가지 뚜렷한 성장 단계를 보여줍니다.
- 유도기: 지수 성장이 시작되기 전의 지연 단계
- 대수기: 세포가 일정한 속도로 분열하는 단계
- 정체기: 성장에 불리한 조건이 되어 세균이 복제를 멈추는 단계
- 사멸기: 세포가 생존력을 잃는 단계
자세히 보기
시료의 광학 밀도(OD)를 측정하는 것은 배양이 어느 성장 단계에 있는지 확인하는 가장 쉬운 방법입니다.
시료를 투명 큐벳 또는 마이크로타이터 플레이트에 넣고 배지 블랭크와 비교하여 빛의 산란 또는 탁도를 측정합니다. 배양 시료가 산란시키는 빛의 양은 세포 농도, 세포 크기 그리고 분광광도계의 구조에 따라 달라집니다. 따라서 관찰된 OD 값으로 세포 농도를 정확히 추정하려면 각 균주별로 분광광도계를 별도로 검교정해야 합니다. 이를 위해 세포 현탁액의 여러 희석액 OD를 측정하고 (위에서 설명한 바와 같이) 해당 연속 희석액의 CFU를 측정하여 배양 밀도와 OD 간의 관계를 나타내는 표준 곡선을 작성합니다(그림 2 참조).
시료를 투명 큐벳 또는 마이크로타이터 플레이트에 넣고 배지 블랭크와 비교하여 빛의 산란 또는 탁도를 측정합니다. 배양 시료가 산란시키는 빛의 양은 세포 농도, 세포 크기 그리고 분광광도계의 구조에 따라 달라집니다. 따라서 관찰된 OD 값으로 세포 농도를 정확히 추정하려면 각 균주별로 분광광도계를 별도로 검교정해야 합니다. 이를 위해 세포 현탁액의 여러 희석액 OD를 측정하고 (위에서 설명한 바와 같이) 해당 연속 희석액의 CFU를 측정하여 배양 밀도와 OD 간의 관계를 나타내는 표준 곡선을 작성합니다(그림 2 참조).
자세히 보기
일반적인 방법:
b. 분광광도계를 적절한 파장으로 설정합니다. 세균의 경우 일반적으로 OD600을 사용합니다.
c. 나중에 세균 현탁액에 사용할 희석액을 적절한 큐벳 또는 마이크로타이터 플레이트에 피펫팅하고 OD600에서 블랭크 측정을 기록하여 적절한 배지로 분광광도계의 0점을 맞춥니다.
d. 세균 균주로 여러 희석액을 만들고 분광광도계를 사용해 각 희석액의 OD600 값을 기록합니다. 이때 세균 성장을 멈추기 위해 얼음을 사용하고 신속히 측정해야 합니다!
e. 위에서 설명한 CFU 방법을 사용해 각 희석액의 세포를 계수하고 OD 측정값을 기준으로 선형 추세선을 추가하여 표준 곡선을 작성합니다.
장점 : 일단 표준 곡선이 작성되면, 이 기법은 매우 빠르고, 비용이 저렴하며, 간단하고, 비교적 세포에 손상을 주지 않으며, 고처리량 측정이 가능하고, 자동화가 용이합니다.
단점: 그러나 분광광도계는 빛의 흡광도를 측정하므로 세포 수를 직접적으로 측정하지는 않습니다. 따라서 OD 측정값과 세포 수를 연결하기 위한 검교정 프로토콜이 필요합니다.
- OD와 세포 수(CFU / mL)를 비교한 표준 곡선을 작성하는 방법은 다음과 같습니다.
b. 분광광도계를 적절한 파장으로 설정합니다. 세균의 경우 일반적으로 OD600을 사용합니다.
c. 나중에 세균 현탁액에 사용할 희석액을 적절한 큐벳 또는 마이크로타이터 플레이트에 피펫팅하고 OD600에서 블랭크 측정을 기록하여 적절한 배지로 분광광도계의 0점을 맞춥니다.
d. 세균 균주로 여러 희석액을 만들고 분광광도계를 사용해 각 희석액의 OD600 값을 기록합니다. 이때 세균 성장을 멈추기 위해 얼음을 사용하고 신속히 측정해야 합니다!
e. 위에서 설명한 CFU 방법을 사용해 각 희석액의 세포를 계수하고 OD 측정값을 기준으로 선형 추세선을 추가하여 표준 곡선을 작성합니다.
장점 : 일단 표준 곡선이 작성되면, 이 기법은 매우 빠르고, 비용이 저렴하며, 간단하고, 비교적 세포에 손상을 주지 않으며, 고처리량 측정이 가능하고, 자동화가 용이합니다.
단점: 그러나 분광광도계는 빛의 흡광도를 측정하므로 세포 수를 직접적으로 측정하지는 않습니다. 따라서 OD 측정값과 세포 수를 연결하기 위한 검교정 프로토콜이 필요합니다.
자세히 보기
직접 현미경 계수법
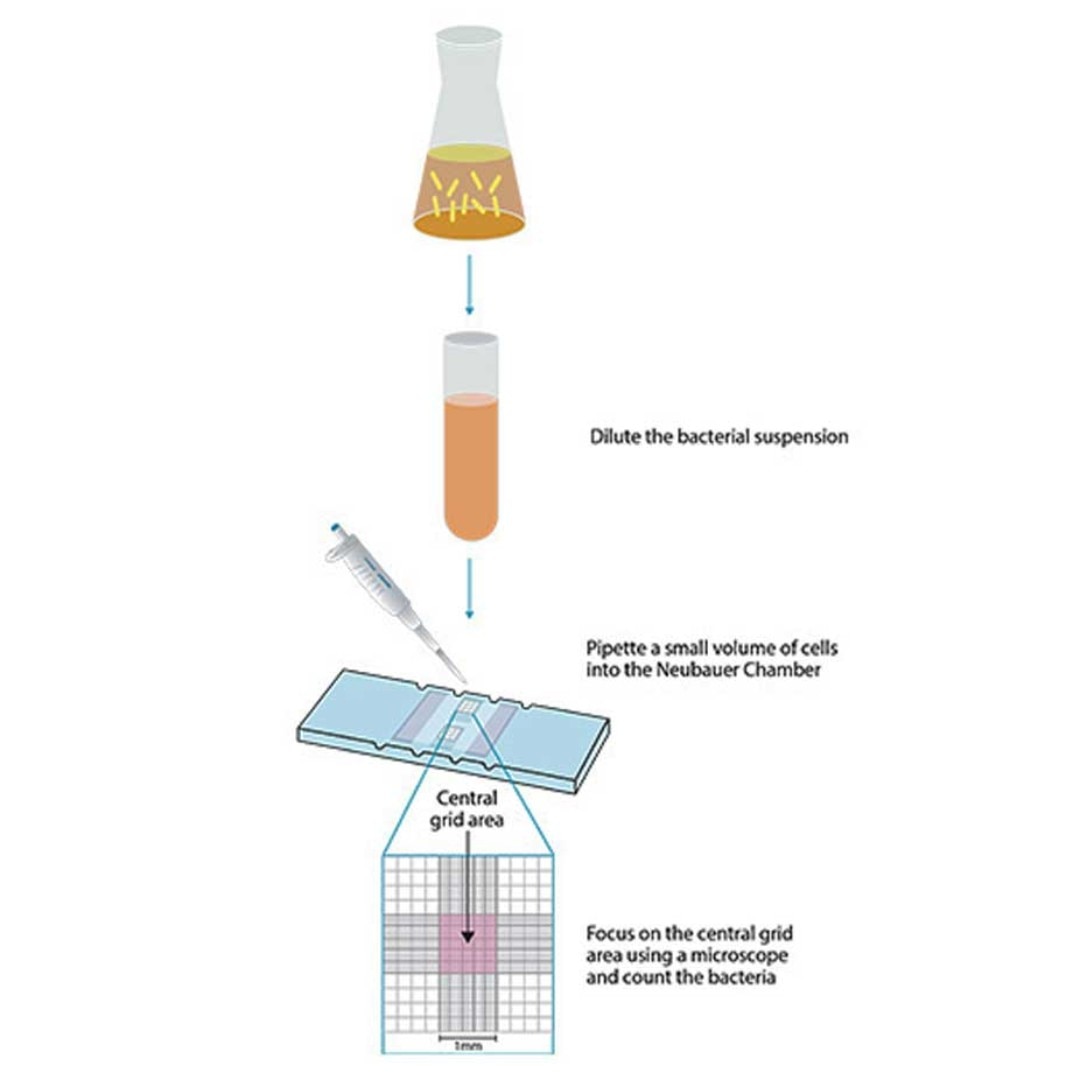
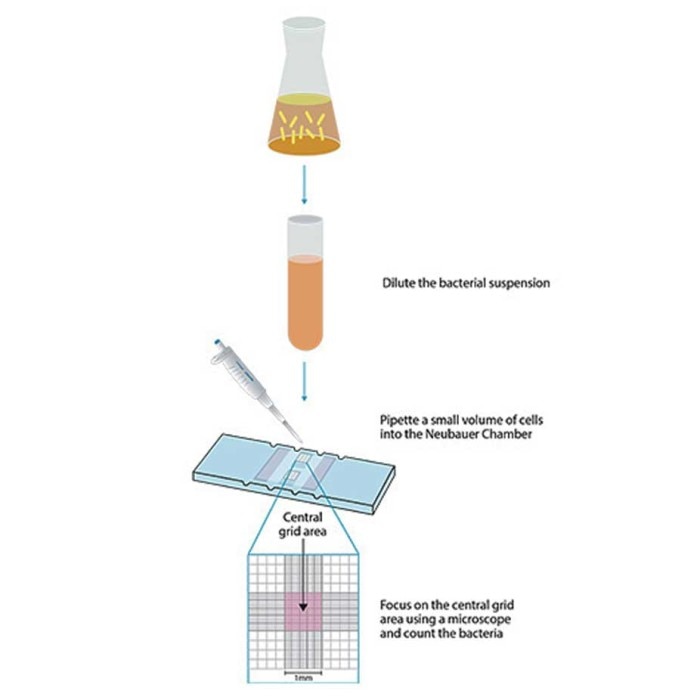
헤모사이토미터는 원래 혈구를 수동으로 계수하기 위해 개발된 계수 챔버 기기입니다1. 현재는 다양한 세포 유형과 응용 분야에서 세균 세포를 포함한 여러 세포 유형의 총 세포 수를 계수하는 데 사용됩니다. 이 기법은 일정한 부피의 액체 배양액 내 세포를 여러 현미경 시야에서 직접 계수하는 방법입니다. 헤모사이토미터는 여러 종류가 있으며, 각기 다른 세포 계수 격자를 가지고 있습니다. 가장 잘 알려진 격자는 'Improved Neubauer' 챔버로, 3×3 mm 크기의 계수 격자가 9개의 1 mm2 정사각형으로 나뉘어 있습니다. 각 정사각형은 다시 16, 100 또는 400개의 더 작은 정사각형으로 나누어져 다양한 크기의 세포를 계수할 수 있는 격자를 제공합니다(그림 3). 챔버의 가장자리는 표시된 격자 위에 일정한 간격으로 특수 유리 커버슬립을 고정할 수 있도록 설계되어 있어 부피를 알 수 있는 구획이 형성됩니다. 표준 '만능' 깊이는 0.1 mm입니다. 이 깊이는 포유류 세포에는 적합하지만, 세균과 같이 작은 세포의 경우 초점을 맞추기가 더 어려울 수 있습니다.
헤모사이토미터는 원래 혈구를 수동으로 계수하기 위해 개발된 계수 챔버 기기입니다1. 현재는 다양한 세포 유형과 응용 분야에서 세균 세포를 포함한 여러 세포 유형의 총 세포 수를 계수하는 데 사용됩니다. 이 기법은 일정한 부피의 액체 배양액 내 세포를 여러 현미경 시야에서 직접 계수하는 방법입니다. 헤모사이토미터는 여러 종류가 있으며, 각기 다른 세포 계수 격자를 가지고 있습니다. 가장 잘 알려진 격자는 'Improved Neubauer' 챔버로, 3×3 mm 크기의 계수 격자가 9개의 1 mm2 정사각형으로 나뉘어 있습니다. 각 정사각형은 다시 16, 100 또는 400개의 더 작은 정사각형으로 나누어져 다양한 크기의 세포를 계수할 수 있는 격자를 제공합니다(그림 3). 챔버의 가장자리는 표시된 격자 위에 일정한 간격으로 특수 유리 커버슬립을 고정할 수 있도록 설계되어 있어 부피를 알 수 있는 구획이 형성됩니다. 표준 '만능' 깊이는 0.1 mm입니다. 이 깊이는 포유류 세포에는 적합하지만, 세균과 같이 작은 세포의 경우 초점을 맞추기가 더 어려울 수 있습니다.
자세히 보기
세균 세포의 경우 'Petroff-Hausser 챔버'라고 불리는 대안 계수 챔버를 사용할 수 있으며, 깊이가 0.02 mm로 더 얕습니다. 이 챔버는 Improved Neubauer 챔버와 동일한 격자를 가지고 있습니다. 또한 Petroff-Hausser 챔버는 두께 1.5 mm의 유리 슬라이드를 갖추고 있어 암시야 현미경 관찰이 가능합니다.
자세히 보기
일반적인 방법:
- 헤모사이토미터로 계수 가능한 세포 농도를 얻기 위해 시료를 (필요한 만큼) 희석합니다.
- 70% 에탄올과 렌즈 페이퍼로 헤모사이토미터 격자를 청소하고 커버슬립을 계수 챔버 위에 부드럽게 올립니다.
- 시료가 대표성을 갖도록 위아래로 몇 번 피펫팅한 후 세포 현탁액의 소량(예: 10 µL)을 격자 챔버 가장자리 근처에 피펫팅하여 모세관 작용(capillary action)으로 세포가 들어가도록 합니다. 세포가 안정될 때까지 1~2분 기다립니다.
- 현미경을 사용해 10X 대물렌즈로 헤모사이토미터 격자선에 초점을 맞춘 후 중앙 1 mm2 정사각형에서 40X 대물렌즈로 세포를 계수합니다(그림 3 참조). 정확한 계수를 위해서는 총 계수가 세포 100개 이상이어야 합니다. 더 작은 정사각형(25개의 세분화된 정사각형)에서는 세포 3개 이상을 목표로 합니다.
- 세포 농도(세포 / mL)는 다음과 같이 계산합니다.
농도 = 세포 수 x 챔버별 증배 계수 x 희석 배수 / 사용한 정사각형의 수
예를 들어, 시료를 1:10으로 희석하고 Petroff 챔버(깊이 0.02 mm)를 사용해 중앙 정사각형(1 mm2)에서 세포 500개를 계수한 경우:
500 x 50,000* x 0.1 /1 = 250,000 CFU / mL
*Petroff 챔버가 깊이는 0.02 mm이고 1 mm² 면적을 커버하므로 한 정사각형의 부피는 0.02 mm3입니다. 0.02 mm3당 세포 수를 mL당 세포 수로 환산하려면 다음과 같이 계산합니다: 1,000/0.02 = 50,000
자세히 보기
장점 : 비용이 저렴하고 비교적 간단하며 소량의 시료만 사용합니다.
단점: 시간이 많이 소요되고 번거로우며 인적 오류가 발생할 가능성이 큽니다.
단점: 시간이 많이 소요되고 번거로우며 인적 오류가 발생할 가능성이 큽니다.
자세히 보기
요약
어떤 방법을 선택할지는 실험의 목적과 상황에 따라 달라집니다. 수중 시료에 존재하는 세균 수를 확인하려는 경우에는 CFU 방법이 적합합니다. E. coli 세포의 회분식 배양을 수행하는 경우에는 OD 측정을 사용하여 배양의 성장 단계를 추적할 수 있습니다. 반면, 후속 분석을 위해 보다 정밀한 측정이 필요한 경우에는 Neubauer 챔버를 사용해 직접 세포를 계수하는 데 시간을 투자해야 할 수 있습니다. 어떤 방법으로 세포를 계수하든지 간에 일관성이 가장 중요합니다! 희석 과정을 사전에 계획하고, 정확하고 신중하게 피펫팅하고, 무엇을 세포로 계수할 것인지에 대해 명확한 기준을 세워야 합니다.
어떤 방법을 선택할지는 실험의 목적과 상황에 따라 달라집니다. 수중 시료에 존재하는 세균 수를 확인하려는 경우에는 CFU 방법이 적합합니다. E. coli 세포의 회분식 배양을 수행하는 경우에는 OD 측정을 사용하여 배양의 성장 단계를 추적할 수 있습니다. 반면, 후속 분석을 위해 보다 정밀한 측정이 필요한 경우에는 Neubauer 챔버를 사용해 직접 세포를 계수하는 데 시간을 투자해야 할 수 있습니다. 어떤 방법으로 세포를 계수하든지 간에 일관성이 가장 중요합니다! 희석 과정을 사전에 계획하고, 정확하고 신중하게 피펫팅하고, 무엇을 세포로 계수할 것인지에 대해 명확한 기준을 세워야 합니다.
자세히 보기
참고 자료:
1. Vembadi, A., Menachery, A. Qasaimeh, M.A. (2019) ‘Cell Cytometry: Review and Perspective on Biotechnological Advances’, Frontiers in Bioengineering and Biotechnology, 7, p. 147. 출처: https://doi.org/10.3389/fbioe.2019.00147
2. Stoddart, M.J. (2011) ‘Cell Viability Assays: Introduction’, in M.J. Stoddart (ed.) Mammalian Cell Viability: Methods and Protocols. Totowa, NJ: Humana Press (Methods in Molecular Biology), pp. 1–6. 출처: https://doi.org/10.1007/978-1-61779-108-6_1.
1. Vembadi, A., Menachery, A. Qasaimeh, M.A. (2019) ‘Cell Cytometry: Review and Perspective on Biotechnological Advances’, Frontiers in Bioengineering and Biotechnology, 7, p. 147. 출처: https://doi.org/10.3389/fbioe.2019.00147
2. Stoddart, M.J. (2011) ‘Cell Viability Assays: Introduction’, in M.J. Stoddart (ed.) Mammalian Cell Viability: Methods and Protocols. Totowa, NJ: Humana Press (Methods in Molecular Biology), pp. 1–6. 출처: https://doi.org/10.1007/978-1-61779-108-6_1.
자세히 보기